所谓化学······乃通过组合那些平平无奇的物质,创造出惊为天人的奇迹。
——【英】波义耳(存疑),近代化学奠基人,$1627-1691$
引言
化学中最为纯粹、朴素的美,并不来自神奇的微观结构、复杂而精密的计算,或者各种令人眼前一亮的理论,而是来自于物质本身的绚丽色彩。或许在很久以后,脑海中那些曾滚瓜烂熟的知识都会被逐渐淡忘,但我永远都会记得那天化学课上,老师掏出的那一大块硫酸铜($\ce{CuSO4}$)晶体给我带来的震撼。

(上图:几大块堪比蓝宝石的硫酸铜晶体,图片来源:@H2元素实验室)
渐渐地,随着知识越学越深,这种神秘的蓝色终究是成为了脑海中的理所当然,最初的那种感觉也便荡然无存了。但是,利用这些知识,我们便可以制得更多美丽的物质,进而弥补这种缺憾。
于是,我决定开启一个新的系列。在这个系列中,我们将会一起动手制造那些美丽的物质,去领略化学最为朴素的魅力。就仿佛是将天上的彩虹收于试管之中,这便是“彩虹收集计划”。而作为这一系列的第一篇文章,当然就要从硫酸铜晶体的幕后正主——铜($\ce{Cu}$)元素开始。
那么,就让我们一起用铜元素,来造就一条彩虹。
正文
酒红色:谢弗勒尔盐

(注:英文名是 $\text{Chevreul’s salt}$,标签上有拼写错误,已在图中改正)
谢弗勒尔盐由法国化学家 $M.~Chevreul$ 于 $1812$ 年首次制得。它是一种混合价态化合物,化学式为 $\ce{Cu3(SO3)2•2H2O}$,含有 $\text{I,II}$ 两种价态的铜,呈现出美丽的酒红色。
为了制得这种物质,我们取五水硫酸铜($\ce{CuSO4·5H2O}$)晶体 $4.8g$ 溶于适量水中,得到蓝色溶液;再取 $4.0g$ 焦亚硫酸钠($\ce{Na2S2O5}$)溶于水中,得到无色溶液。在剧烈搅拌下混合两种溶液,很快便可以看到溶液颜色变成了美丽的翠绿色:

这种翠绿色的东西究竟是何方神圣,直到今天也没人说得清(个人猜测是铜与焦亚硫酸根的络合物)。总之,加热溶液后绿色迅速变浅,随之而来的是一种细碎的红色沉淀析出,即谢弗勒尔盐。此处将溶液转移至锥形瓶中后静置半天,瓶底也出现了一大坨红色沉淀:

干燥后这种沉淀颜色加深,最终呈现出酒红色。这种色调在铜盐的身上确实比较罕见,反倒与氧化亚铜($\ce{Cu2O}$)比较接近。这种物质受热并不稳定,在 $200^{\circ}C$ 以上分解放出 $\ce{SO2}$,以此可以鉴定之。我们最终得到了 $4.53g$ 产物,产率约 $61\%$(事实上再放一会应该可以沉淀出更多)。
\[\ce{3CuSO4 + 4Na2S2O5 ->[\Delta]Cu3(SO3)2•2H2O\downarrow+ 4Na2SO4 + SO2\uparrow+ H2SO4}\]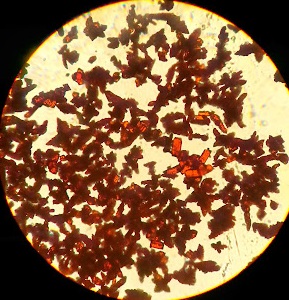
(上图:显微镜下的谢弗勒尔盐晶体)
在红色的铜化合物中,谢弗勒尔盐算是容易制备的一种,但它又没有氧化亚铜那种类似砖头渣子的感觉。反倒是它的晶体结构异常复杂,一直到 $1965$ 年才被完全搞清楚。它的身上还有很多谜团等着我们去发掘。
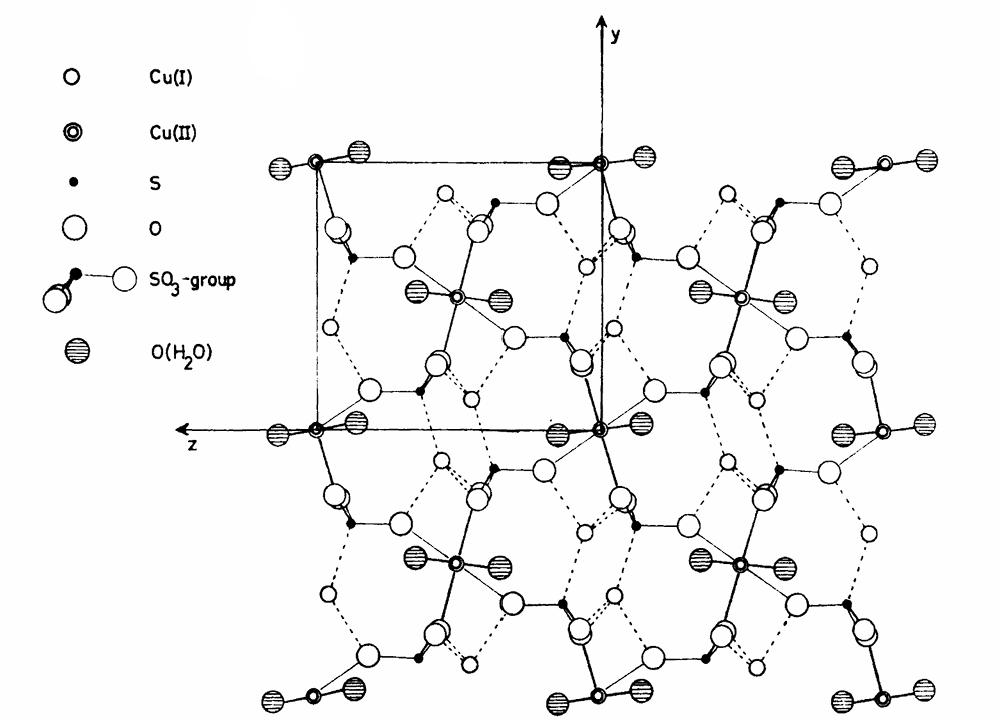
(上图:谢弗勒尔盐的晶体结构手稿)
暗橙色:铬酸铜

铬酸铜是一种难溶于水的暗橙色物质,化学式为 $\ce{CuCrO4}$。制备这种物质非常简单,但由于需要用到剧毒的铬酸钾($\ce{K2CrO4}$),所以请勿在不能保证自身安全的情况下进行此实验。
我们取 $10g$ 五水硫酸铜溶于适量水中,得到蓝色溶液;再取 $7.7g$ 铬酸钾,溶于水中形成橙黄色溶液。随后混合两者,立刻就能看到大量橙色沉淀析出:
\[\ce{CuSO4 + K2CrO4 -> CuCrO4\downarrow + K2SO4}\]
一个有趣的发现是,如果使用铬酸溶液(即将三氧化铬($\ce{CrO3}$)溶于水得到的溶液)代替铬酸钾溶液,那么一开始溶液会变成绿色但仍然澄清,向其中加几滴碱后出现大量黄色沉淀。黄色和绿色交织在一起,使得整个体系变得难以描述。虽然在溶液中两者之间的颜色差异非常明显,但在抽滤、烘干之后颜色就与资料上铬酸铜的颜色一致了:

我个人的猜测是,在 $\text{pH}$ 比较低的条件下,溶液中的 $\ce{Cr(VI)}$ 以重铬酸根的形式存在,可能会与 $\ce{Cu^{2+}}$ 形成类似于 $\ce{[Cu(Cr2O7)2]^{2-}}$ 的配合物从而导致了溶液的绿色。由于没有仔细研究,不敢保证这一猜想一定正确,如果各位大神有确切知道的还请评论告知。
总之,干燥后的铬酸铜呈现出沉稳的暗橙色。在第一次使用 $\ce{K2CrO4}$ 的实验中,我们总共得到了 $6.4g$ 铬酸铜,产率约 $89.1\%$。在工业上,铬酸铜被用于陶瓷的制作,也可以利用其受热分解的性质,将其加工成亚铬酸铜($\ce{Cu(CrO2)2}$),即著名的 $\text{Adkins-Lazier}$ 催化剂。也正是因此,如果在烘干时温度设定太高且时间过长,那么产物会部分变黑,从而影响成色。
橙黄色:二水合氯铜酸(二)吡啶鎓
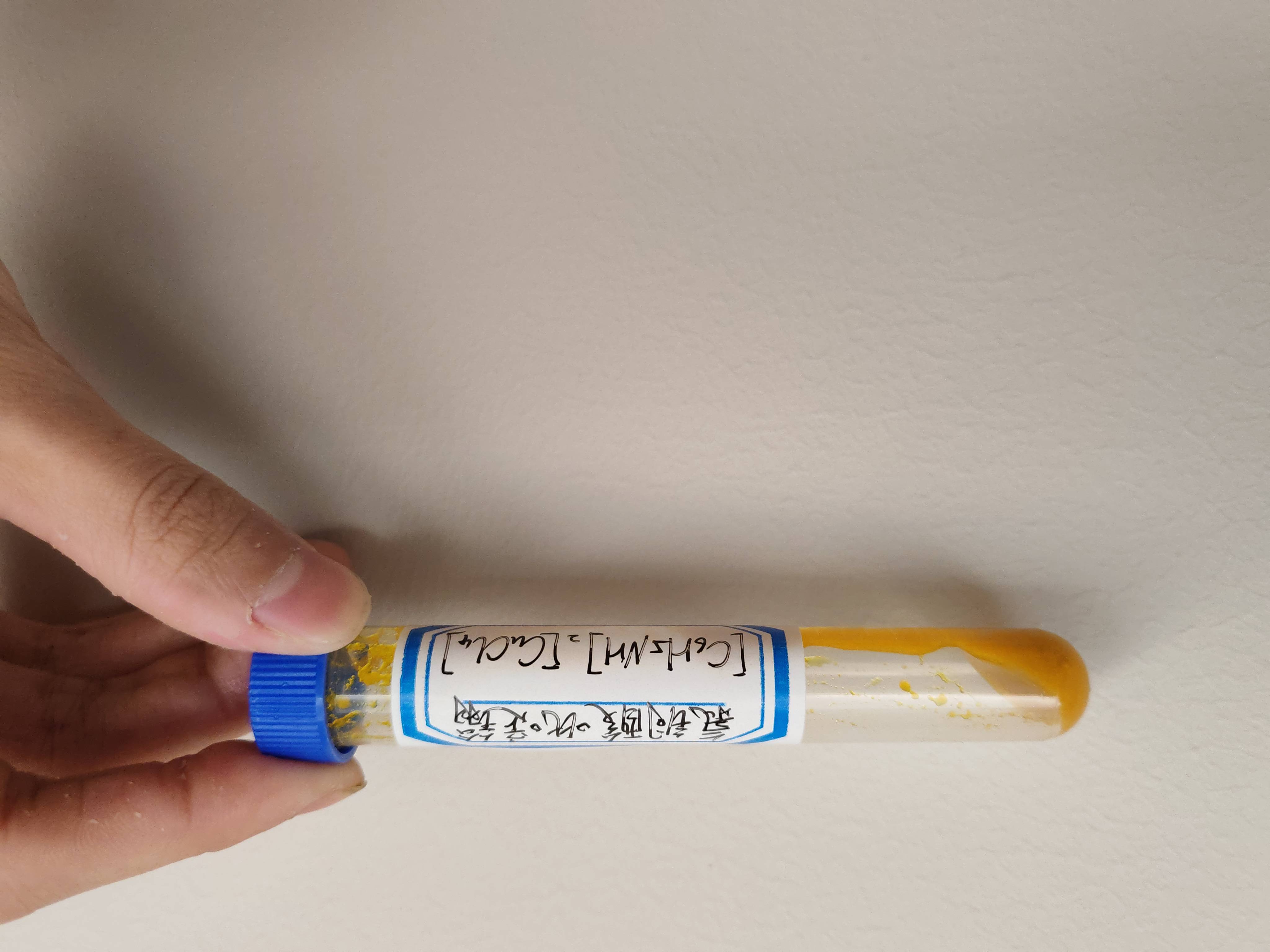
二水合氯铜酸二吡啶鎓是一种橙黄色物质,化学式为 $\ce{(C6H5NH)2(CuCl4)·2H2O}$(上图标签上没写结晶水)。这种色调实际上来自于阴离子,即四氯合铜酸根($\ce{CuCl4^{2-}}$),阳离子只是来跑个龙套。当然,由于四氯合铜酸钠这样的氯铜酸盐从水溶液中无法得到,所以也不能说阳离子没有作用。如果没有吡啶,可以换成二乙烯三胺($\ce{C4H13N3}$,缩写 $dien$)之类的有机胺,或者是体积超大的铯离子($\ce{Cs+}$),也可以得到颜色类似的产物。
为制取该物质,我们取 $2g$(量比较少,当然也可以加量)二水合氯化铜($\ce{CuCl2·2H2O}$),并将其溶于浓盐酸中,得到绿色溶液:

(注:由于实验中忘记拍摄了,所以上图是网图。实际上如果只取 $2g$ 氯化铜的话不需要那么多溶剂)
随后量取约 $1mL$ 吡啶($\ce{C6H5N}$,室温下呈液态),逐滴加入绿色溶液中。溶液并不会发生明显的变色。接着便是静置等待溶剂蒸发,产物结晶。这一步骤至少要等半天,没有那么多时间的我只好加热浓缩。浓缩过程要注意剩余的水量,等到水没多少就需要关火了,因为如果继续加热下去它就会原地分解,放出吡啶和氯化氢,最后只剩下氯化铜:
\[\ce{(C6H5NH)2(CuCl4)·2H2O->[\Delta] 2C6H5N\uparrow + 2HCl\uparrow + 2H2O\uparrow + CuCl2}\]在一开始,我还高估了这玩意的稳定性,打算把它扔进烤箱里烘干,但即使设定温度只有 $50^{\circ}C$,分解依旧无可避免,放出的吡啶让整个烤箱都充斥着那种难以描述的烂哈密瓜味。没办法,只能让它自由风干,但用这么个玩意一直占着通风柜会引起众怒,所以我只好在未完全干燥的情况下就将其装管(所以产率也没法算了)。根据资料,如果一直让它自由蒸发可以得到非常美丽的橙黄色晶体,就像下图中一样:

最后的提醒:由于吡啶具有不容忽视的毒性,所以请勿在简陋的条件下进行此实验。由于产物在温度稍高时便可以持续向周围环境释放吡啶,所以应储存于低温密闭环境中。
鹅黄色:水合氧化亚铜

是的,你没有看错。所谓氢氧化亚铜($\ce{CuOH}$),即实际上的水合氧化亚铜($\ce{Cu2O·H2O}$)是可以在室温下稳定存在的,而且相比同族下面那个氢氧化银($\ce{AgOH}$)稳定到不知道哪里去了。
我们可以用类似于制取谢弗勒尔盐的方法制取该物质,只不过这次焦亚硫酸钠(或者用亚硫酸钠($\ce{Na2SO3}$)替代之)需要过量。实际操作中我们仍取用 $4g$ 焦亚硫酸钠,但五水硫酸铜只取了 $2g$。如果你不想为了这个实验霍霍那么多试剂,也可以使用一个巨山寨的方法,那就是手动滴加氢氧化钠溶液将反应体系的 $pH$ 调整至中偏碱性,这样还原剂的用量就可以少一点。混合溶液后依旧是显示出绿色,但这次我们不加热它,而是向其中兑入酒精($\ce{C2H5OH}$,工业级的即可)。几乎是酒精加进去的瞬间,一种脏黄色的细颗粒沉淀立刻生成,即水合氧化亚铜:

(上图:抽滤中的水合氧化亚铜,下方滤液依然很脏,所以需要多次过滤)
由于颗粒细小,我们需要用不同孔径的滤纸进行多次抽滤。最后得到的黄色物质置于表面皿中风干,其颜色会逐渐变浅,最终得到淡黄色到鹅黄色的水合氧化亚铜:

(上图:干燥中的水合氧化亚铜)
此处切不可用烤箱烘干,因为这货在室温下还勉强稳定,一旦加热立刻脱水,甚至如果周围环境干燥的话不需要加热它就会脱水,导致颜色变深、变红,完全脱水就会变成棕红色的氧化亚铜。我们做了好几次实验,但每次做出来的成品都和上一次做出来的有一点颜色差别,可能就是这个原因。最后的产率在 $40\%$ 左右。
孔雀石绿色:二水合一水一(尿素)四-桥-(乙酸根)合二铜
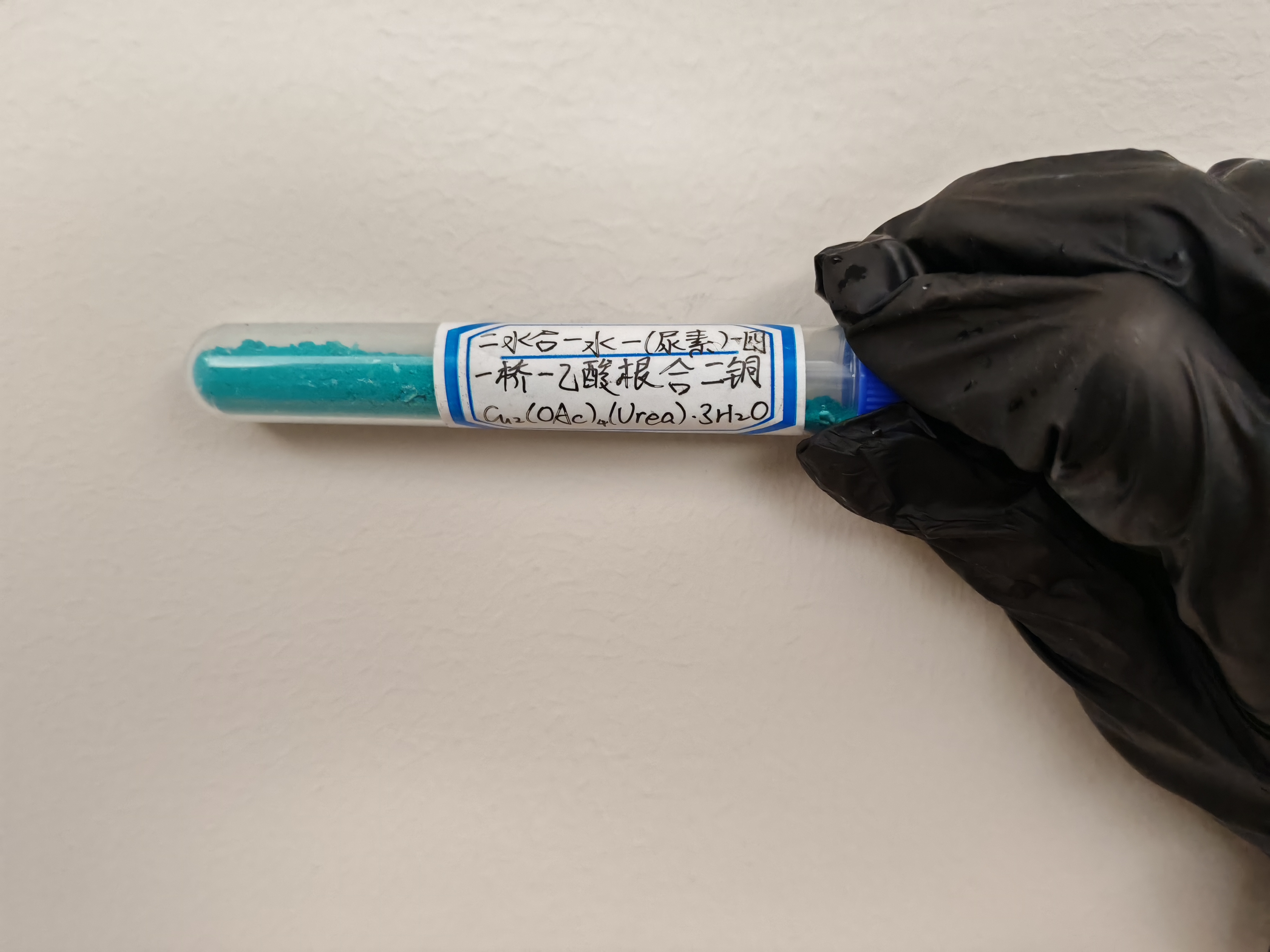
绿色到蓝色算是二价铜配合物的经典色调了,所以我在纠结了很久之后才选出了这么个名字冗长的东西。选择这货一是因为原料便宜且易得,二是作为前化竞生在试题中与这货碰到过很多次,而这次终于有机会见到它的真实面貌。
首先称取 $6.25g$ 五水硫酸铜,再称取 $9g$ 尿素($\ce{CO(NH2)2},\text{Urea}$),随后将两者全部装入烧瓶中。注入约 $25mL$ 水,随后设定温度 $60^{\circ}C$,加热搅拌至其全部溶解。在此情况下,尿素与铜离子首先配位,得到 $\ce{[Cu(Urea)4]^{2+}}$ 离子:
\[\ce{[Cu(H2O)4]^{2+} + 4 Urea ->[\Delta] [Cu(Urea)4]^{2+} + 4H2O}\]
只不过由于 $\ce{[Cu(Urea)4]^{2+}}$ 也是蓝色的,用肉眼并不好分辨配体交换是否已经完成,所以这一步最好多加热一会,不然最后的产率就会很感人(此处虽反应物添加较少,也需保温 $1h$ 左右)。趁着加热的时间,我们称取 $6.8g$ 三水合乙酸钠($\ce{CH2COONa·3H2O}$,简写 $\ce{NaOAc·3H2O}$),并在加热结束后将其加入反应体系。仔细观察,可以看到溶液颜色逐渐改变(时间取决于乙酸钠颗粒大小),先是变成深蓝色,然后逐渐变绿,并开始变得浑浊:
\[\ce{2[Cu(Urea)4]^{2+} + 4AcO- + 3H2O -> [Cu2(OAc)4(Urea)(H2O)]·2H2O\downarrow + 7Urea}\]
溶液中析出的细小孔雀石绿色晶体就是我们的目标产物。为使其充分反应,我们维持 $60^{\circ}C$ 加热和搅拌一个小时。反应结束后取下烧杯,置于冰柜中冷却以促使产物析出。充分冷却后进行抽滤,用冰水(大冬天的水本来就很冰)洗涤数次后将滤饼转移至表面皿中,送入烤箱中烘干。此处,烘干温度不宜太高($80^{\circ}C$ 以下),否则产物可能失去结晶水甚至在内部直接发生氧化还原反应,进而分解得到一大堆乱七八糟的物质:
\[\ce{[Cu2(OAc)4(Urea)(H2O)]·2H2O ->[\Delta] 2CuOAc + 3C + Urea + CO\uparrow + 6H2O\uparrow}\](实际反应分好几步,此处是整合的方程式)
.png)
(上图:产物滤饼,图片来源于网络,实际没做出那么多(哭))
最终得到产物 $5.72g$,产率约 $47.9\%$。作为双核配合物,$\ce{[Cu2(OAc)4(Urea)(H2O)]·2H2O}$ 具有典型的“中国灯笼”式结构,四个乙酸根做桥连配体,如下图:
(photo:lost)
另外,如果我们不用乙酸钠,而是用乙二酸四乙酸二钠($\ce{EDTA·2Na}$)螯合,其他步骤均不变,则最终得到的是一种浅蓝色的单核配合物 $\ce{Cu(EDTA)(Urea)2·H2O}$,其中的 $\ce{Cu^{2+}}$ 离子六配位,$\ce{EDTA}$ 做四齿配体,且它的四个配位原子在同一平面上。尿素和铜也有一些有趣的配合物,在此不做详述。
青色:二倍半水合柠檬酸铜

青色的二倍半水合柠檬酸铜($\ce{Cu3(C6H5O7)2·2.5H2O}$)是一种微溶于水的铜盐,由于拍摄问题它与上面那货颜色看起来差不多,但实际上还是有很大差别的,尤其是二者放在一起的时候。由于变态般的晶体结构,柠檬酸铜也是化竞试卷上的常客,但一旦从试题中走出来,它的美丽青色绝对是铜彩虹中最令我喜欢的。
制取柠檬酸铜非常简单。首先取 $7.5g$ 五水硫酸铜,加适量水溶解;再取 $5.9g$ 二水合柠檬酸三钠($\ce{Na3C6H5O7·2H2O}$,若是其他水合状态保持摩尔数),加适量水溶解,随后在搅拌中将柠檬酸钠溶液倒入硫酸铜溶液中。可以观察到溶液颜色变深、变暗,可能是生成了配合物导致:

(上图左:加入柠檬酸钠溶液之前;上图右:加入柠檬酸钠溶液之后)
随后开始加热。溶液颜色逐渐变浅且逐渐变得浑浊,这是因为配合物结构被破坏,柠檬酸铜逐渐析出。保温一段时间使反应完全,最终悬浊液会变成青色:
\[\ce{3Cu^{2+} + 2C6H5O7^{3-} + 2.5H2O->[\Delta] Cu3(C6H5O7)2·2.5H2O\downarrow}\]
随后抽滤该溶液,并用水和乙醇洗涤。得到的滤饼置于表面皿中,送入烤箱烘干。如果烘干温度设定过高,可能导致产物的脱水,得到亮蓝色的二水合柠檬酸铜和绿松石色的一水合柠檬酸铜,温度再高可能导致内部复杂的氧化还原反应。

(上图:表面皿中的二倍半水合柠檬酸铜)
最终得到 $4.7g$ 产物,产率约 $\ce{76.5\%}$。最后,如果想要制取另外两种水合状态的柠檬酸铜,最好的方法并不是加热脱水,因为火候很难把握。有意者可以自行阅读附于最后的参考文献 $[3],[4]$,在此不再赘述。
蓝色:水合二草酸合铜酸钾

水合二草酸合铜酸钾($\ce{K2[Cu(C2O4)2]·nH2O}$,上图标签中笔误了)作为一种经典的微溶钾盐,可能是这些物质中最为人熟知的一个。相比于五水硫酸铜,它的颜色更深一点。根据溶解度可以更好地区分二者。
制备这种物质也非常简单。首先称 $10g$ 五水合硫酸铜、$18g$ 氢氧化钾($\ce{KOH}$)、$18g$ 二水合草酸($\ce{H2C2O4·2H2O}$,直接用草酸钾代替后两个也可以),分别配置成溶液。首先混合后两份,由于酸碱中和剧烈放热,连加热都可以免了。随后在搅拌下混合硫酸铜溶液,观察到溶液蓝色变深,标志着配合物生成;溶液随即变得浑浊,细小的结晶颗粒析出:

(上图左:刚加入硫酸铜溶液时溶液颜色变深;上图右:搅拌一会后溶液变混)
此时的溶液在昏暗的环境下用光照射,可以看到蓝晶雨的现象,只不过效果貌似没有甘氨酸铜($\ce{[Cu(NH2CH2COO)2]·H2O}$)来得好(而且忘记拍摄了)。随后冰水浴骤冷,但继续搅拌。之所以这样,是因为这货有两种水合形式:二水合二草酸合铜酸钾($\ce{K2[Cu(C2O4)2]·2H2O}$),片状结晶,湛蓝色;四水合二草酸合铜酸钾($\ce{K2[Cu(C2O4)2]·4H2O}$),针状结晶,蓝色,颜色较前者更浅。此处搅拌、骤冷可以使二水合物更多析出,从而使产物颜色更深(我觉得那样更好看点)。若想真正分离二者,则需要数次重结晶。
随后进行抽滤。为除去降温后同时析出的硫酸钾,需要用冷水多次洗涤。完成后将其转移至表面皿中,送入烤箱干燥。烤箱温度不宜超过 $100^{\circ}C$,否则产物会失水变为无水物,进一步升温还会导致内部氧化还原反应的发生。最终得到产物 $10.2g$,产率(以二水合物记)约为 $72\%$。
紫色:二水合盐酸二(乙二胺)合铜

二水合盐酸二乙二胺合铜($\ce{[Cu(en)2]Cl2·2H2O}$,上图标签中省略了结晶水)是此次计划中的最后一种物质,呈现出美丽的紫色。需要注意,合成该物质所需的乙二胺($\ce{NH2CH2CH2NH2,en}$)是管制化学品,请不要在非正规实验室中擅自尝试该实验。
为合成此物质,我们首先取 $6g$ 二水合氯化铜配置成溶液(溶剂用蒸馏水),再量取 $4.7mL$($0.352mol$) 室温下为液态的乙二胺(如果只有乙二胺溶液的话加等摩尔即可)。在搅拌的同时混合两者,溶液的颜色会逐渐变紫、变深,最终得到的溶液近乎于黑色。将溶液转移至结晶皿(大烧杯也行)中,加热蒸发溶剂:

(上图:结晶皿中正在蒸干的 $\ce{[Cu(en)2]Cl2}$ 溶液)
由于这货在水中溶解度很大,不蒸干溶剂根本结不出晶来。也正是因此,原料中的乙二胺最好不要用盐酸乙二胺($\ce{en·2HCl}$)来替代,否则你得先加氢氧化钠(之类的碱)游离出乙二胺,但与此同时反应体系中会多出 $\ce{NaCl}$ 的杂质。它难以除去,会随着溶剂蒸干被一起析出来。当然,如果你只是想看个色儿,对产物纯度没有任何要求,那用盐酸乙二胺倒也无妨。
一直蒸到水快没了的时候,鲜艳的紫色晶体才会出现在器皿中:

(上图:未完全干燥的 $\ce{[Cu(en)2]Cl2·2H2O}$ 晶体。图片来自网络)
接着就可以把它送进烤箱。由于比之前那些东西都稳定些,所以烤箱的温度也可以设定得比较高,但由于晶体间存在大量水,整个干燥的过程依旧让人咬牙切齿。干燥完成后,便得到了最终的产物。最终产率超过 $95\%$,算是非常可观。
最后的意外收获?
在上述所有实验都做完之后,我本想再制备一次水合氧化亚铜(因为前几次的产率实在是有点低),结果不知道搭错了哪根筋,我忘记了焦亚硫酸钠应当过量,在反应体系还是酸性的情况下就把酒精怼了进去。出乎意料的是,一种和溶液颜色差不多的沉淀立刻生成。我马上进行了抽滤,留在漏斗上的是一种闻所未闻的浅绿色物质:

(注:中间白色的是磁力搅拌器的磁子)
用酒精洗涤数次后滤饼颜色并未改变。我将其转移至表面皿中,由于事发突然,表面皿并没有干燥,所以部分物质被浸润并变为了蓝色:

(上图:置于表面皿中的该物质,可以看到部分被水浸润的变为了蓝色)
随后将其在烤箱内烘干。一段时间后我打开烤箱,居然发现这种物质变成了美丽的天蓝色(难道是失去了结晶水?可是设定温度也不高啊)。将其装管后,我更加确信它的颜色发生了变化:

(上图:最终得到的天蓝色物质)
这个东西究竟是什么?显然不可能是水合氧化亚铜或谢弗勒尔盐,毕竟颜色差距实在是太大了。或许是硫酸铜?但它的颜色看起来比五水硫酸铜浅得多(难道是硫酸铜的其他水合状态?)。况且,那个奇妙的变色应该如何解释呢?在查阅了一堆文献后,我依然没有找到满意的答案。
突然间,我感受到了一种前所未有的乐趣。在一个看起来如此简单的反应体系中,我创造出了一种超越我认知的物质,更何况它还有着令人着迷的美丽颜色。我下定决心,要搞清楚这家伙是何方神圣。或许结果会让人大跌眼镜,但又或许,它真的是某种未被详细记录过的物质呢?
毕竟,所谓化学,便是通过组合那些平平无奇的物质,创造出惊为天人的奇迹。
彩虹全家福
在文章的末尾,当然要附上一张物质全家福。除了上面介绍的八种铜化合物以及最后意外做出来的那个未知物质外,还有同批实验做出来的 $6$ 种化合物,由于不含 $\ce{Cu}$ 元素所以没有在正文中介绍。你能猜到它们都是什么吗?

参考文献
论文类
$[1]$:Kierkegaard, Peder et al. “The Crystal Structure of Cu2SO3.CuSO3.2H2O.” Acta Chemica Scandinavica 19 (1965): 2189-2199.
$[2]$:叶钊 and 张汉辉. “〔Cu2(OAc)4(Ur)(H2O)〕(H2O)2的合成和光谱及热稳定性的研究.” (1994).
$[3]$:Palčić A, Halasz I, Bronić J. Crystal structure of copper(ii) citrate monohydrate solved from a mixture powder X-ray diffraction pattern. Powder Diffraction. 2014;29(1):28-32. doi:10.1017/S0885715613001267
$[4]$:Donald. Mastropaolo, Dana A. Powers, Joseph A. Potenza, and Harvey J. Schugar Inorganic Chemistry 1976 15 (6), 1444-1449
书籍类
(1)Gmelin Handbook of Inorganic and Organometallic Chemistry - 8th edition
(2)Chemistry of the Elements (Second Edition), N. N. Greenwood and A.Earnshaw
(3)《无机合成》,R. W. Pary 主编,申泮文等译