谨以此文,纪念天然橡胶真实结构被人类破译100年;纪念酚醛树脂工业化先驱,美国杰出的化学家贝克兰逝世80周年。
几年前,英国皇家化学学会评选在过去 $1$ 个世纪中“改变世界的5项化学发明”,最后上榜的是青霉素类药物、合成氨、聚乙烯、孕酮和液晶显示。其中,聚乙烯($-[CH_{2}-CH_{2}]-_{n}$)作为塑料的主力之一,在今天的生活中早已不可或缺,也是高分子化学对人类的重要贡献。

(上图:改变世界的 $5$ 项化学发明,来自英国皇家化学学会)
高分子化学,自诞生以来不过 $100$ 年,但其发展之快令其他几乎所有学科都望尘莫及,各种高分子材料令人目不暇接,已然成为现代社会不可或缺的部分。所谓高分子,即是由很多重复结构单元通过共价键结合而成的大分子。巨大的分子量使得高分子具有复杂的结构、复杂的溶液行为、特殊的粘弹性以及其他强大的性能。
事实上,早在古代,人们的生活就已和天然高分子物质结成了息息相关的关系。高分子物质支撑着人们的吃穿住各方面,作为人类食物的淀粉,以及纺织为衣物的棉、毛、丝等都是天然的高分子物质。但对其真正的系统性研究却是近代的事。$1872$ 年,德国化学家贝耶尔($1835-1917$)首次合成了酚醛树脂,也是第一个人造高分子物质。合成反应如下:

(注:虽然在此之前,人类已经会将天然高分子改性,但贝耶尔是第一个把小分子聚成高分子的人,即他首次完成了聚合反应)
只可惜,贝耶尔却并没有继续关于这种物质的实验,这也使得直到 $1907$ 年,改良后实用性强的酚醛树脂才被美国化学家贝克兰($1863-1944$)发明并投入市场。但此时,人们还错误地认为高分子是环状聚集的分子。
$1920$ 年,是为高分子化学元年。有机化学家,高分子之父施陶丁格在这一年发表了高分子化学开山之作《论聚合》,质疑了环状高分子结构,并在 $1922$ 年提出了链状高分子结构。与他并肩作战的是另一位化学家毕克斯,他在无数次实验后于 $1924$ 年明确指出:天然橡胶是由小分子(顺式异戊二烯)聚合而来的链状大分子。
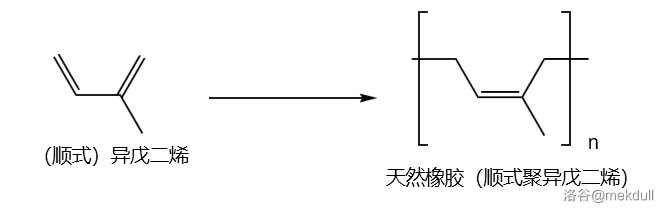
(上图:天然橡胶的链状结构,最早由毕克斯在 $1924$ 年指出)
虽然在现在,这个结构已经被所有选科化学的人熟知,但在 $100$ 年前,毕克斯和施陶丁格的观点却是以一己之力对抗时代。直到 $20$ 世纪 $30$ 年代,他们的观点才被世人接受。
$1922$ 年,塑料的代表——聚乙烯被首次合成。$1933$ 年,人们发现乙烯可以在高压下聚合为聚乙烯,这类反应随后被命名为加聚反应(加成聚合反应)。乙烯的加聚反应如下图所示:
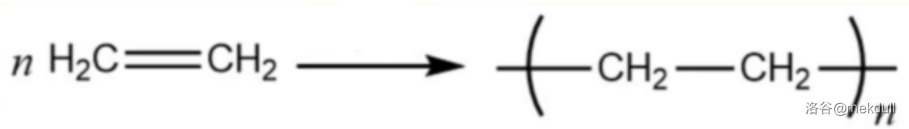
虽然已经投入生产,但直到 $1953$ 年,齐格勒和纳塔才发明了低压下催化生成聚乙烯的方法,即著名的齐格勒-纳塔聚合反应。反应机理如下:

齐格勒-纳塔聚合开启了配位络合聚合的大门,开创了定向聚合的新领域。两人因为高分子化学领域的卓越贡献而获得了 $1963$ 年的诺贝尔化学奖。
除了配位络合聚合以外,自由基聚合也是一种被广泛应用的聚合模型。典型的例子如“塑料王”聚四氟乙烯($PTFE$)的生产,这种高分子是在 $1938$ 年由美国科学家普伦凯特首次合成的,并被当做耐腐蚀材料用在了曼哈顿计划中。今天制备 $PTFE$ 的工艺是四氟乙烯($C_{2}F_{4}$)的聚合,以过硫酸钾($K_{2}S_{2}O_{8}$)作为引发剂:
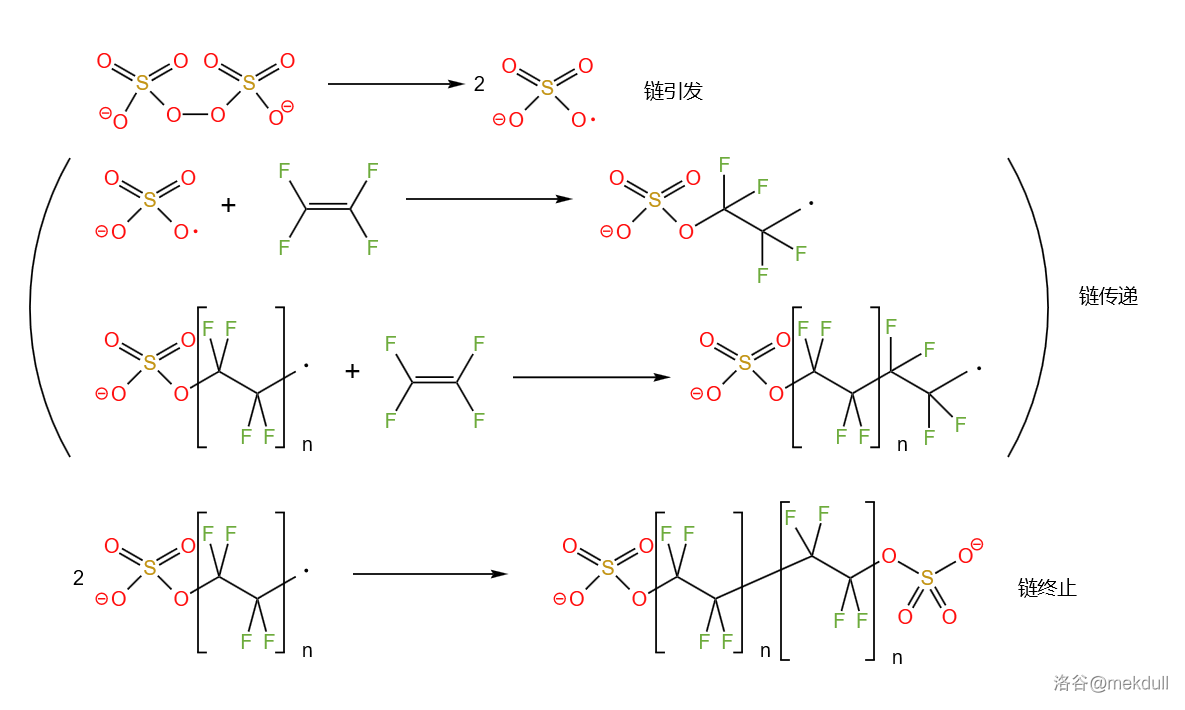
而原料四氟乙烯的制备一般是以氯仿($CHCl_{3}$)为原料,经过 $HF$ 高温处理得到:

聚四氟乙烯耐酸(包括王水等混酸在内)、耐碱,化学性质非常稳定,甚至可以在一定程度上耐 $F_{2}$ 的腐蚀,尽管价格相对昂贵,但依然在防腐方面、电子电气方面、医疗方面、建筑方面以及实验室中得到了广泛的应用。
另一种(或者说一类)化学稳定性出众的高分子材料是硅橡胶,它在 $1945$ 年首次被美国化学家合成。直链硅橡胶的结构通式如下:

其中,最简单的甲基硅橡胶($MQ$,通式中 $R=CH_{3}$)的制备一般采用环状化合物聚合的方法。以 $Si$ 粉与一氯甲烷($CH_{3}Cl$)为原料制得二氯二甲基硅烷($Si(CH_{3}){2}Cl{2}$),随后在酸催化下聚合为环状的八甲基环四硅氧烷($(Si(CH_{3}){2}O){4}$),最后在催化剂作用下聚合:

硅橡胶常温下为固体,但常温下为无色液体的硅油与它的通式是相同的。两者之所以有此差别,是因为硅油的聚合度($n$)比较低,分子量也比较低,因此呈现液态。这告诉我们,高分子从来都是量变引起质变的过程,随着 $n$ 增大,分子可以从气态小分子变成液态,超过某一个阈值之后再变成固态的大分子。由于硅橡胶主链由高强度的 $Si-O$ 键构成,所以它具有很出色的耐高、低温性能,且化学性质稳定,这也赋予了它的生理惰性,因而在各个领域得到广泛应用。
高分子的结构一定是一条条长链吗?或许也不那么一定。早在 $1839$ 年,硫化橡胶就被美国化学家古德伊尔($1800-1860$)在无意间制取了出来。天然橡胶虽具有弹性、防水等优异性能,但遇热发粘、遇冷发硬,难以广泛应用。这是因为天然橡胶中有不饱和的碳碳双键,容易被氧化变质。但用硫处理后,双键被加成,链与链之间形成交联结构,从而大大改善橡胶的性质:
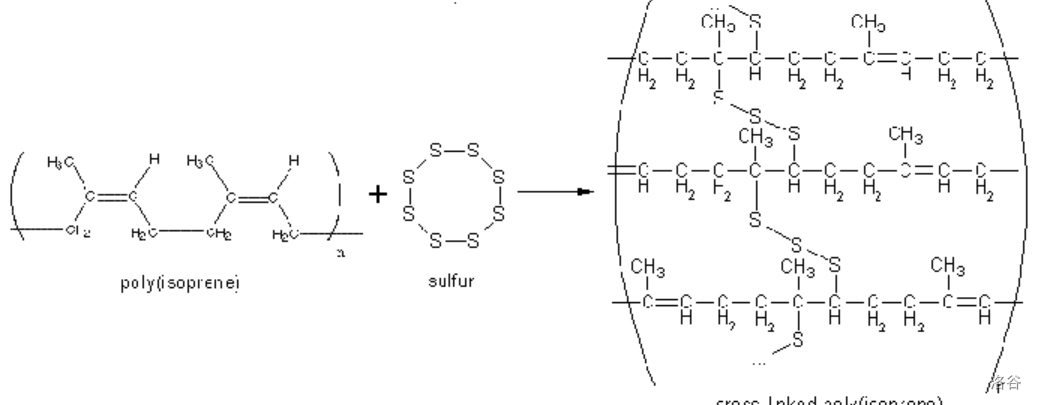
硫化之后,整体结构变成了网状,链之间由 $S-S$ 键牢固地连接在一起。目前,我们在生活中已经难以见到天然橡胶了,而我们所说的“橡胶”一般指的就是硫化橡胶。
除了硫化形成交联结构,我们还有许多方法得到网状高分子。下面就是一例,利用正硅酸乙酯($Si(OCH_{3})_{4}$)作为交联剂,可以得到一种改性的硅橡胶:

随着越来越多的高分子材料被合成,我们需要一套理论描述高分子的结构与性质的关系。$1948$ 年,美国化学家弗洛里与哈金斯提出了 $Flory-Huggins$ 高分子溶液理论,将高分子溶液体系考虑为“似晶格”体系处理,获得了巨大的成功。从此,高分子的微观结构与宏观性质有了联系,他们也因此获得了 $1974$ 年的诺贝尔化学奖。
$1956$ 年,美国化学家 $Szwarc$ 提出了活性聚合的概念,从此让高分子材料进入了分子设计时代。活性聚合是指在适当的合成条件下,无链终止与链转移反应,活性中心浓度保持恒定的时间比完成反应所需时间长数倍的聚合反应。利用这种聚合反应,我们可以设计出性质特殊的多组分聚合物。SBS弹性塑料就是典型例子,它的名字实际是 $Styrene-Butadiene-Styrene$ (苯乙烯-丁二烯-苯乙烯)的缩写,其典型结构如下:
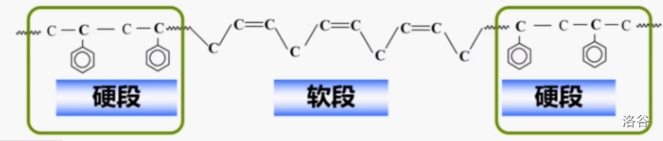
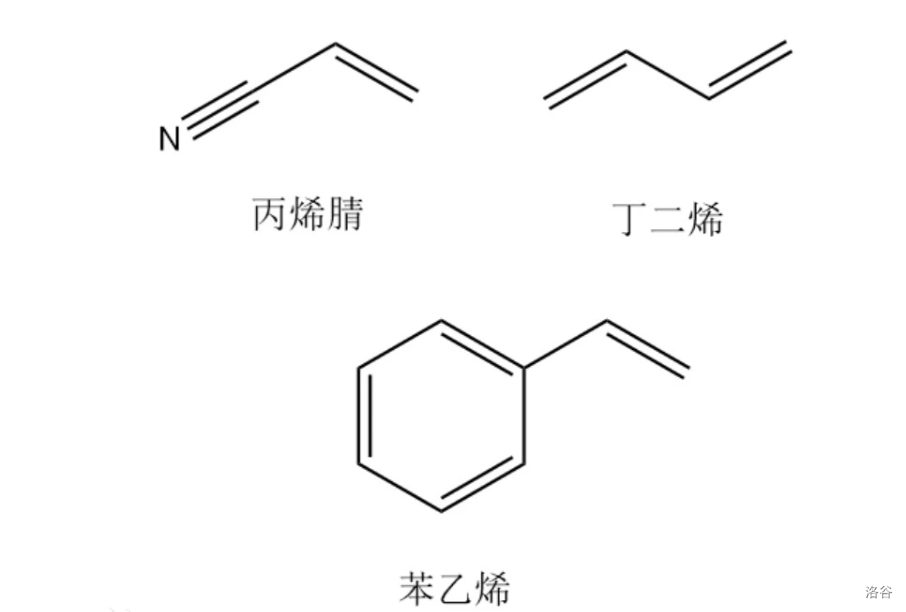
由于聚苯乙烯比较“硬”,而聚丁二烯比较“软”,软硬交织就可以形成性质特殊的弹性材料。类似的例子还有很多,比如汽车保险杠使用的 $ABS$ 树脂材料,就是由丙烯腈($A$),丁二烯($B$)与苯乙烯($S$)三组分聚合而成的。
$20$ 世纪 $70$ 年代以后,导电高分子作为新兴领域发展了起来。最早的导电高分子是聚乙炔。事实上,早在 $1960$ 年,就已经有科学家把乙炔聚合了起来,但得到的是一种黑色的固体,也不能导电。$1967$ 年,一位印度的访问学者来到日本化学家白川英树的实验室准备将乙炔聚合,但(可能是因为白川英树英语发音不太标准)他在制备过程中却一不小心使用了 $1000$ 倍标准量的齐格勒-纳塔催化剂,导致最后制取出来的是一种银白色、具有金属光泽、能导电的固体。我们现在所说的聚乙炔就这么误打误撞被发现了。聚乙炔单链的结构如下:
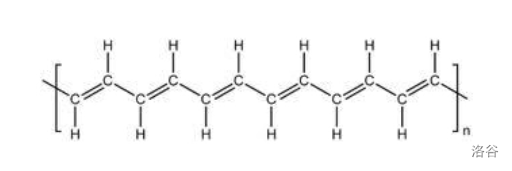
后续研究证明了,由于催化剂量太大,造成聚乙炔过度结晶,形成了纤维状结构,从而具有了导电性。白川英树和另外两位科学家因为导电高分子的开创性研究而获得了 $2000$ 年的诺贝尔化学奖。目前,导电高分子材料已经在能源、电池、传感器、电子器件等领域得到了极为重要的应用,成为了信息时代的基石材料之一。
可以说,高分子材料在过去一百年里极大地改变了人类生活。但是,对高分子材料的广泛应用也带来了一些问题。由于高分子材料一般都化学性质稳定,难以被降解,尤其是塑料类物质造成的“白色污染”已经极为严重,这也是人类亟需解决的问题之一。
高分子仍然在蓬勃发展。它会不会在未来再一次改变世界?拭目以待吧。